Revista Digital Universitaria ISSN: 1607 - 6079 | Publicación mensual
1 de mayo de 2013 vol.14, No.5
• PRESENCIA UNIVERSITARIA •
Introducción
El desarrollo actual de la Nanociencia y la Nanotecnología no seria posible sin la caracterización a través de técnicas de identificación de materiales, tales como la microscopia electrónica de barrido, de transmisión o de fuerza atómica. Además, es necesario conocer las propiedades de los materiales: estructura, composición, morfología, propiedades térmicas, etc., para posteriormente darle aplicación específica a los mismos.En la síntesis de nuevos materiales, las propiedades de éstos dependen no sólo de las propiedades de los materiales de partida, sino también de su morfología y las características interfaciales, por lo que es muy importante su determinación.
Asimismo, la caracterización de un catalizador es el aspecto más importante en la investigación y desarrollo de catalizadores. El área superficial, la elucidación de la estructura, composición y propiedades químicas, tanto de los sólidos utilizados en la catálisis heterogénea como de los compuestos absorbidos y los intermediarios presentes en la superficie del catalizador durante la reacción, son de vital importancia para entender la relación entre las propiedades del catalizador y la actividad catalítica.
Sin embargo, cabe mencionar que muchos programas de estudio de licenciatura contienen un mínimo de asignaturas de caracterización de materiales, nanomateriales y catalizadores. Es por ello que este trabajo tiene como objetivo presentar un material básico, que permita al lector introducirse con mayor facilidad a la investigación en estas áreas.
El trabajo consitió en hacer una revisión de las técnicas más comunes de caracterización de materiales, nanomateriales y catalizadores. Una vez seleccionadas, se procedió, en primer lugar, a presentar los acrónimos; se realizó un análisis de la información obtenida de la aplicación de las técnicas y se hizo un listado de los tipos de materiales en los cuales se aplican. Adicionalmente, se describió el principio básico, así como la instrumentación y métodos. Finalmente, para que el lector se familiriarice con las técnicas, se presentan ejemplos en los que se discute, en la terminología adecuada, el ánalisis del espectro, patrón de difracción de rayos X, curva térmica, isoterma, micrografía, etc.
En la tabla 1, se resumen las técnicas explicadas en el libro.
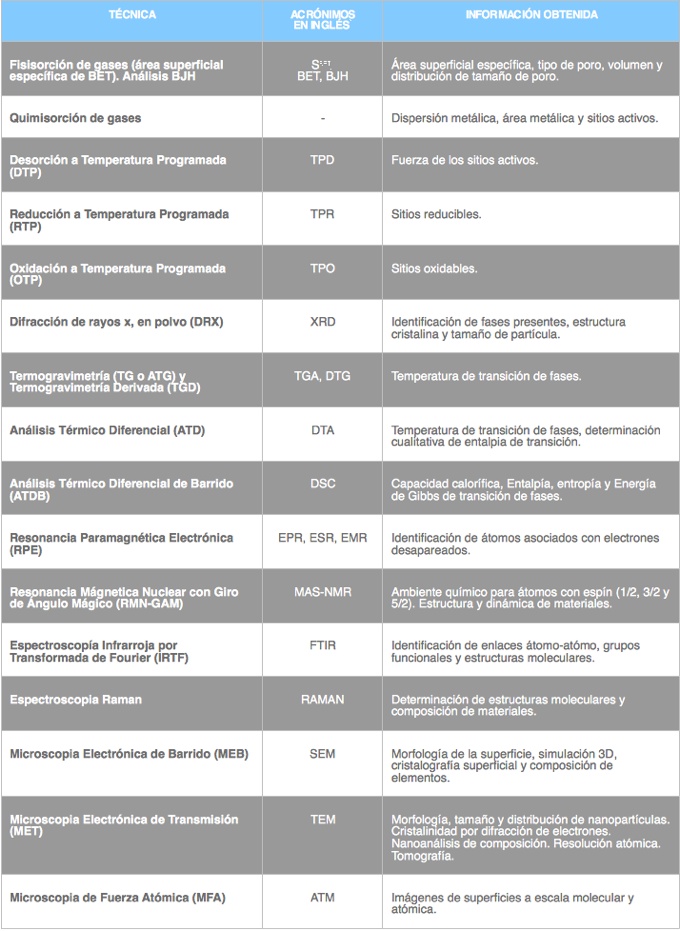
Tabla 1 a S: specific surface area; BET: Brunauer-Emmet-Teller; BJH: Barrett-Joyner-Halenda; TPD; temperature programmed desorption; TPR: temperature programmed reduction; TPO: temperature programmed oxidation; XRD: X-ray diffracction; TGA: thermogravimetric analysis; DTG: derivative thermogravimetry; DTA: differential thermal analysis; DSC: differential scanning calorimetry; EPR: electron paramagnetic resonance; ESR: electron spin resonance; EMR: electron magnetic resonance; MAS-NMR: magic angle spinning nuclear magnetic resonance; FTIR: Fourier transform infrared spectroscopy; RAMAN: Apellido del físico hindú C.V. RAMAN; SEM: scanning electron microscope; TEM: transmission electron microscope; ATM: Atomic force microscopy;
Técnica: Resonancia paramagnética electrónica
A continuación, los autores nos permitimos presentar, de forma resumida, el contenido de una de las técnicas, con algunas referencias seleccionadas.AcrónimosRPE (Resonancia Paramagnética Electrónica).
EPR (Electron Paramagnetic Resonance).
ESR (Electron Spin Resonance).
EMR (Electron Magnetic Resonance).
Información obtenida y áreas de aplicación
- Identificar átomos asociados con electrones desapareados.
- Elucidar estructuras de intermediarios y especies absorbidas.
- Definir estados de oxidación de metales de transición, con capas d o f parcialmente llenas Fe+3, Mn+2, Cu+2, Cr+3, V+4, etc.
- Establecer estado de espín.
- Determinar concentración de especies paramagnéticas.
- Estudiar la simetría de cristales.
- Defectos en cristales.
- Mecanismos de reacción vía radicales libres. (Gómez-Vidales et. al., 2010)
- ROS (Especies reactivas de Oxígeno, por ejemplo, radical hidroxilo y anión superoxido), NOS (Especies reactivas de nitrógeno, por ejemplo, óxido nítrico). (Tsuchiya et. al., 2003).
- Antioxidantes (Frontana et. al., 2004; dos Santos et. al., 2009).
- Catalizadores.
- Materiales conductores.
- Compuestos orgánicos.
- Fibra de vidrio.
- Defectos de radiación y dosimetría (Juárez-Calderón et. al., 2009).
- Cristales líquidos.
- Metales de transición (Olguín et. al., 2006).
- Metales complejos.
- Establecer el estado de espín.
- Alimentos.
- Enzimas.
- Co-enzimas.
- Lípidos y proteínas (Borbat et al., 2003).
- Vitaminas (C, E, K).
- NADHP.
- Hemoglobina.
- Compuestos organomagnéticos.
- Atrapadores de radicales libres (Yoshiro et. al., 2003; dos Santos et. al., 1999).
- Inmunoensayos.
- Agentes cancerígenos.
- Minerales.
- Polímeros conductores.
- Fibras de carbono.
Estado de la muestra
Pueden llevarse a cabo mediciones en soluciones liquidas o sólidas, polvos, monocristales, gases y soluciones congeladas (vidrios).Cantidad requerida de la muestra
Esta es una técnica no destructiva, generalmente se requieren de 1 mg a 10 mg de muestra, dependiendo de la respuesta paramagnética de cada sistema.Principio básico
Clásicamente, un electrón puede considerarse como una esfera —cargada negativamente— girando. Debido a su carga negativa, esta rotación produce una corriente circulante en la dirección contraria a la rotación de la esfera. La corriente produce un campo magnético en la vecindad del electrón, el espín del electrón puede considerarse un pequeño imán. En los átomos o moléculas neutras, los pequeños magnetos (imanes) forman pares magnéticamente neutros, por lo tanto, no existe un momento magnético neto en la mayoría de los materiales (átomos o moléculas diamagnéticas). No así en las moléculas, donde se encuentra, por lo menos, un electrón desapareado. Esta característica la convierte en una especie paramagnética.Las propiedades magnéticas de los electrones no apareados están definidas por los siguientes parámetros:
- Momento Angular de espín (S).
- Número cuántico de espín (s).
- Número cuántico magnético (M).
- Magnetón de Bohr.
- Momento magnético.
- Factor de desdoblamiento espectroscópico o valor g.
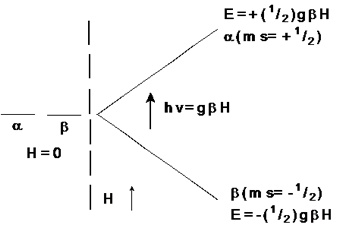
Figura 1. Efecto Zeeman electrónico. Los sistemas examinados deben ser paramagnéticos (con electrones impares). Las diferencias de energía que se estudian en la espectroscopia de RPE se deben a la interacción de electrones desapareados, en la muestra, con un campo magnético estático externo. Este efecto es llamado efecto Zeeman electrónico (Abraham & Bleaney, 1970; Wertz & Bolton, 1986), el cual es la energía que produce diferentes estados de espín bajo la influencia de un campo magnético estático externo H (en la dirección z), posteriormente, los electrones del primer estado de espín por absorción de un cuanto de energía de microondas son excitados al siguiente nivel energético, cambiando la dirección del espín por la absorción de energía de microondas. Esto sucede cuando se cumple la condición ΔE=hv= gβH. El fenómeno de absorción de energía de microondas es la RPE. Figura 1.
- Los dos estados de espín (+1/2, -1/2) tienen la misma energía en ausencia de un campo magnético H.
- Las energías de los estados del espín magnético divergen linealmente cuando aumenta el campo magnético.
- De aquí es importante obtener el valor g (factor espectroscópico, adimensional) que nos da información sobre las características del electrón desapareado.
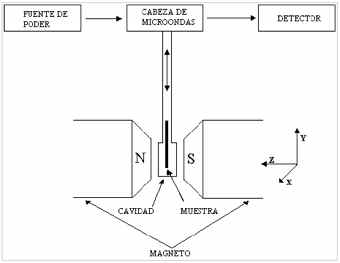
Figura 2. Principales componentes del espectrómetro de Resonancia Paramagnética Electrónica.
Instrumentación y métodos de cálculo
Los constituyentes más importantes en todo espectrómetro de RPE (Figura 2) son: a) fuente de microondas; b) guía de ondas; c) cavidad resonante, en la cual se coloca la muestra a estudiar; d) un campo magnético uniforme, en el cual se introduce la cavidad resonante con la muestra; e) un detector para la medida de absorción de la energía de microondas dentro de la cavidad; f) un sistema de modulación del campo magnético estático y g) un amplificador look-in para la presentación del espectro obtenido (Wertz & Bolton, 1986).Frecuencia de resonancia
Los equipos de RPE trabajan en diferentes frecuencias, conocidas como bandas (Tabla 2). La banda X y la banda Q son las frecuencias de mayor uso.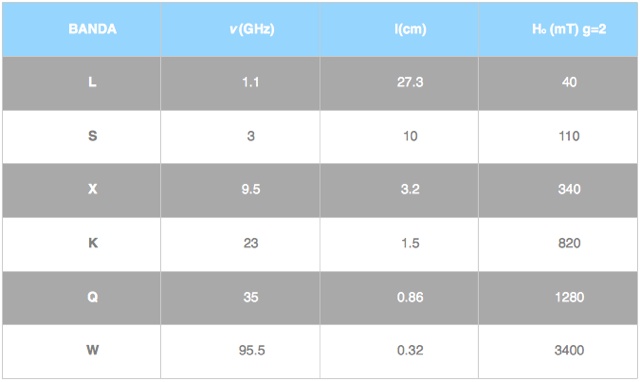
Tabla 2 Valores de campo para g=2 en las diferentes bandas en RPE.
Presentación del espectro
El espectro de RPE se presenta comúnmente como la primera derivada de la curva de absorción, la cual se grafica contra la fuerza del campo magnético (H). Es fácil diferenciar entre la curva de absorción y la primera derivada, la primera de ellas es una curva ancha. El principal inconveniente de la curva de absorción es que no es fácil identificar las señales cuando se presentan acoplamientos finos e hiperfinos. En cambio, en la primera derivada, la curva cruza la abscisa en el punto máximo de la curva de absorción (ver figura 3); el número de picos y hombros en la curva de absorción se pueden determinar por el número de mínimos (marcados con asterisco) o máximos en la curva derivada.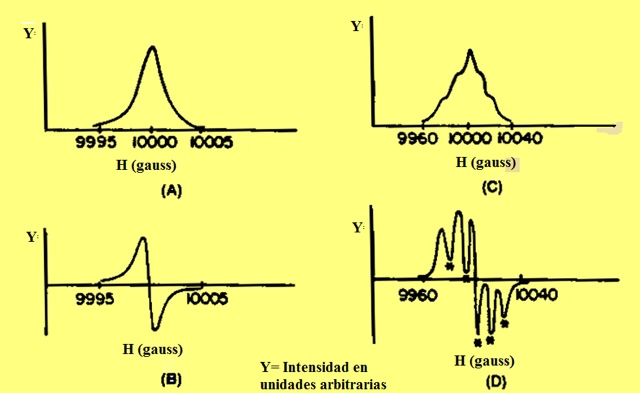
Fifura 3 A y C corresponden a la curva de absorción de un espectro sin desdoblamiento hipérfino; B y D a la 1ª derivada de un espectro con acoplamiento hiperfino, respectivamente.
Por lo tanto, el espectro de RPE es una gráfica de intensidad de absorción en unidades arbitrarias (Y), graficado contra campo magnético H (mT o gauss). A partir de los espectros de RPE se obtiene información sobre la estructura fina (S) y los siguientes parámetros: factor espectroscópico (g), constante de acoplamiento hiperfino (A), constantes de campo cristalino (D y E), distancia pico-pico (L), y el ancho de línea (Γ). Si las condiciones experimentales son favorables, también es posible determinar constantes de acoplamiento superhiperfinas (shfcc).
Ejemplos
a) Estudio de minerales por RPE.
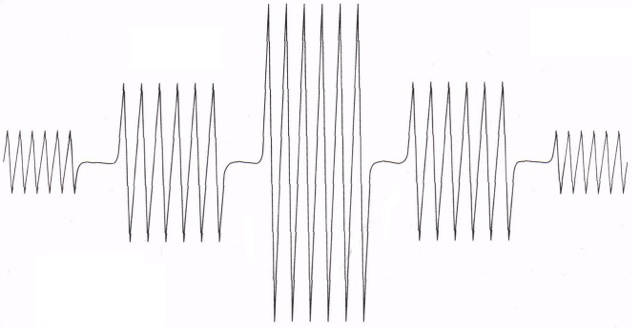
Fifura 4 Espectro RPE de Mn2+ de tremolita natural, mostrando una combinación de estructura fina (5 grupos de picos) y desdoblamiento hiperfino (cada grupo se subdivide en 6 picos).
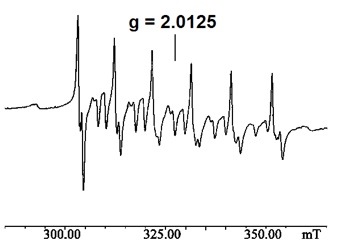
Figura 5. Ampliación de la señal central del espectro de RPE, de M-HSO3CF3.Como ejemplo, la figura 4 muestra el espectro de RPE, debido a la detección de pequeñas cantidades de Mn2+ en tremolita natural, donde se observan 5 grupos de señales debido al espín electrónico S=5/2 (d5) y el doblamiento de cada juego de señales en 6 picos, debido a la interacción con el espín nuclear de IMn=5/2 (Golding et. al., 1972).
Otro ejemplo, es el espectro de una arcilla tratada con ácido tríflico (M-HSO3CF3): muestra seis líneas anisotrópicas bien definidas, con g = 2.0125 y constante de acoplamiento hiperfino A = 9.66 mT, típicas de iones Mn+2, debida a la transición central +1/2 →-1/2. En adición exhibe dobletes débiles (Figura 5) entre los componentes hiperfinos principales, que son asignados a transiciones prohibidas causadas por distorsión axial del campo cristalino, en ausencia de acoplamiento dipolar. (Vargas-Rodríguez et. al., 2008)
Conclusión
Lo anterior referido es una lectura de caracter introductorio, con rigor científico, que está enfocada a diversas cuestiones sobre la caracterización de materiales, nanomateriales y catalizadores. El libro del que se extrae la información consta de 190 páginas y 50 figuras que ejemplifican la aplicación de diversas técnicas analíticas. Aunque, originalmente, fue concebido para estudiantes de licenciatura de carreras del área de Química que revisan estos temas, a través de las presentaciones en congresos, consideramos que también puede servir de material de apoyo para estudiantes de posgrado y/o investigadores que deseen incorporarse a la investigación en el área de materiales, nanomateriales y catalizadoresAgradecimientos
Se agradece el apoyo económico del Proyecto PAPIME PE103907: Iniciación Temprana a la Investigación en el Área de Fisicoquímica (catálisis y materiales) y de los proyectos: PAPIIT IN 104808 y PAPIIT IT1039123. Agradecemos además la asistencia técnica del Q. Jaime Pérez-Huerta y del Q. Raymundo Garduño Monroy.Bibliografía
ABRAHAM, A. and Bleaney B. Electron Paramagnetic Resonance of Transition ions. Claredon Oxford. 1970.
BORBAT, P.P., Costa, -Filho, A., Mosciki, J.K. and Freed, J.H. Electron Spin Resonance in studies of membranes and proteins, Science. 291, 266-269. 2003.
DOS SANTOS, A. B., et. al. “Antioxidant Properties of Plant Extracts: an EPR and DFT Comparative Study of the Reaction with DPPH, TEMPOL and Spin Trap DMPO”. J. Braz. Chem. Soc., 20, No. 8, 1483-1492. 2009.
FRONTANA, C., Frontana-Uribe, B. A. and González, I. Electrochemical and ESR study on the transformation process of α-hidroxy-quinones. J. Electroanal. Chem. 573, 307-314. 2004.
GOLDING, R. M., Newman, R. H., Rae, A. D. and Tennat, W.C. Single crystal EPR study of Mn2+ in natural tremolite. J. Chem. Phys. 57, 1912-18. 1972.
GóMEZ-VIDALES, V., et. al. Basic medium oxidation of aromatic α-hidroxy-ketones: a free radical mechanism. J. Mol. Struct. 963, 115-121. 2010.
JUáREZ-CALDERÓN, et. al. Study of dosimetric properties of acetylsalicylic acid in Pharmaceutical preparations by EPR spectroscopy. J. Radioanal. Nucl. Chem, 280, 245-249. 2009.
OLGUIN, J., et. al. Self assembly of a hybrid organic-inorganic dicopper (II) coordination polymer with a calix [4] arene derived nitrogenous ligand. Inorg. Chem Commun. 9, 1096-1098. 2006.
TSUCHIYA K., et. al. New methods to Evaluate endothelial function: Endothelial function by Hemoglobin-Nitric Oxide Complex using Electron Paramagnetic Spectroscopy. J. Pharmacol. Sci. 93, 417-422. 2003.
VARGAS-RODRíGUEZ, Y. M., et. al. Caracterización espectroscópica, química, morfológica y propiedades superficiales de una montmorillonita mexicana. Revista Mexicana de Ciencias Geológicas, 25 (1)134-144. 2008.
WERTZ, J. E. and Bolton, J. R. Electron spin resonance: elementary theory and practical applications. Chapman and Hall. 1986.
YOSHIHIRO, Y., Tomoko, I., Hiroyuk, N. and Hiroaki, K. Evaluation of Free Radical Scavenging Activities of Antioxidants with an H2O2/NaOH/DMSO System by Electron Spin Resonance. J. Agric. Food Chem. 47, 4653-4656. 1999.
COMENTARIOS
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO
Dirección General de Cómputo y de Tecnologías de Información y Comunicación
Dirección General de Cómputo y de Tecnologías de Información y Comunicación
2013 Esta obra está bajo una licencia de Creative Commons